来源:CBG资讯
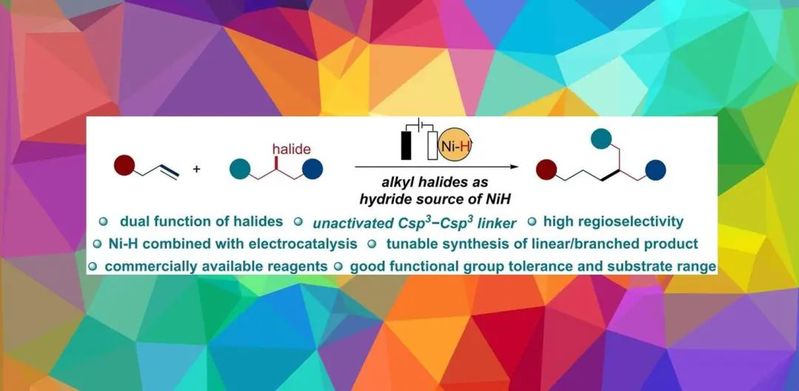
Csp3–Csp3键普遍存在于天然产物、药物和功能性有机分子中,因此构建此类化学键是合成有机化学、药物化学和相关领域最具吸引力的策略之一。过渡金属催化的交叉偶联反应是构建Csp3–Csp3键的有效的方法,但是通常需要使用有毒且敏感的有机镁、有机锌或有机锡试剂,这在某种程度上限制了这种方法的实际应用。Kolbe电解是一种可以避免使用有机金属试剂构建Csp3–Csp3键的重要方法,该方法可以使简单的烷基羧酸通过直接电化学阳极脱羧偶联构建Csp3–Csp3键。然而,由于所需的高电流密度和较差的选择性,Kolbe反应在有机合成中的实际应用仍然受限。
在过去的几十年中,有机电催化已发展成一种可以解决过去难以解决的问题有的效方法。最近,Baran课题组实现了交流电催化的Kolbe反应(图1a)和氧化还原活性酯(RAE)与过渡金属催化剂镍在还原条件下的脱羧交叉偶联这两种新型的构建Csp3–Csp3键的方法。另外,林松组报道了在电化学条件下使用两种不同烷基卤化物在无过渡金属条件下通过SN2过程构建Csp3–Csp3键的反应(e-XEC)(图1b)。但底物中必要的活化基团(Bpin、Ph、SiMe2Ph)限制了这种方法在合成化学中的广泛应用。
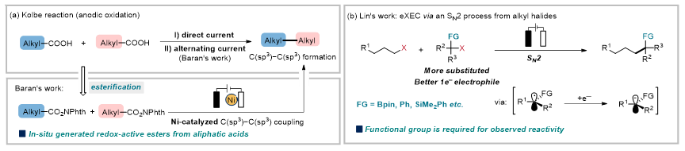
图1. 电化学Csp3–Csp3键的构建策略。
相比卤化物,烷基烯烃同时具有高原子经济性和多样的反应性等特点,在构建Csp3–Csp3键方面表现出显著的优越性。然而,其固有的低反应活性使得其官能转化十分困难,而且,之前的相关研究通常需要添加化学计量的硅试剂作为氢源,或者需要加入金属锰还原剂,很明显这不利于反应规模扩大或工业应用。因此,如果用电催化方法可以克服这一限制,将会使这种合成Csp3–Csp3键的策略更具发展潜力。
新葡的京集团3512vip元素有机化学国家重点实验室仇友爱课题组聚焦于有机电化学的研究,特别是亲电试剂的电化学还原交叉偶联(Angew. Chem. Int. Ed. 2023, e202306679),基于课题组前期以及电化学还原羧化、电化学还原氘化的工作(Angew. Chem. Int. Ed. 2022, 61, e202207746;Angew. Chem. Int. Ed. 2023, 62, e202214710,Nat. Commun. 2022, 13, 3774)。近日,学院仇友爱和南京大学王敏燕课题组联合报道了电化学条件下Ni-H催化的烷基卤化物和烷基烯烃的交叉偶联反应。反应有以下特点:a)卤化物同时作为偶联底物和氢源;b)可以避免使用硅烷作为氢源以及添加还原性金属试剂;c)良好的化学选择性和区域选择性,可以实现线性和支链偶联产物的可调合成;d)底物范围广,对一些天然产物和药物分子也表现出良好的耐受性。
论文信息:
Electrochemical NiH-Catalyzed C(sp3)−C(sp3) Coupling of Alkyl Halides and Alkyl Alkenes
Pengfei Li, Guangsheng Kou, Tian Feng, Prof. Dr. Minyan Wang, Prof. Dr. Youai Qiu
Angewandte Chemie International Edition
DOI: 10.1002/anie.202311941




